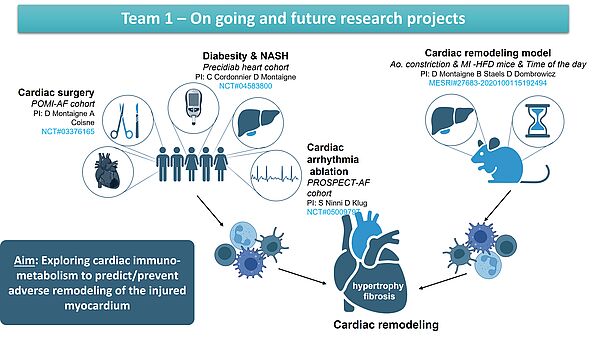
Groupe Coeur - Pr Bart Staels
Présentation de la recherche thématique
Comme dans de nombreux domaines de soin aux patients, l’abandon d’une approche « taille unique » au profit d’une approche individualisée de « médecine de précision » représente l’avenir proche et raisonnablement réalisable du traitement des maladies cardiovasculaires. L’objectif ultime de la médecine cardiaque personnalisée est de fournir des soins médicaux et des résultats optimisés pour chaque individu, en fournissant une meilleure thérapie à chaque patient en termes d’efficacité, de sécurité et de réduction des coûts associés.Nos activités de recherche sont ainsi dédiées à la médecine personnalisée pour prévenir et cibler les maladies cardiovasculaires grâce à
- De nouveaux biomarqueurs d'imagerie,
-
Le séquençage de l’ADN des leucocytes circulant et myocardiques,
-
Le phénotypage de l’immuno-métabolisme du myocarde,
-
La quantification (avec des capteurs aptamères GFET) de biomarqueurs cardiaques dans des échantillons biologiques (sang, salive, sueur, air exhalé) de patients dont les niveaux sont très bas, voire actuellement indétectables.
Notre recherche translationnelle, qui s’étend des modèles de rongeurs aux patients, vise à améliorer la compréhension de la pathophysiologie du remodelage cardiaque, à affiner la stratification du risque cardiovasculaire et la stratégie thérapeutique associée au bénéfice/risque, non seulement chez les patients ayant des antécédents de maladie cardiovasculaire, mais aussi chez les patients présentant des facteurs de risque cardiovasculaires tels que le tabagisme, le diabète de type 2, une dyslipidémie et l’obésité, même en l’absence d’antécédents ou de symptômes médicaux cardiovasculaires.Nos projets se concentrent plus spécifiquement sur la fonction, le métabolisme énergétique et le remodelage cardiaque chez les patients souffrant de diabète et/ou de valvulopathie cardiaque, et visent à améliorer la stratification des patients et à développer une médecine cardiovasculaire personnalisée.
Cliquez-ici, si vous souhaitez avoir plus d'informations.
Mots-clès
Remodelage cardiaque ; valvulopathies, arythmie ; fibrillation atriale ; métabolisme énergétique ; communication inter-organes ; immuno-métabolisme ; imagerie cardiaque.

COISNE Augustin
PU-PH – Cardiologie
augustin.coisne[@]chu-lille.fr
ORCID : 0000-0002-1662-7874
Le Pr Augustin COISNE (MD, PhD, HDR) est cardiologue (thèse de médecine en 2013). Il occupe un poste de Professeur des Universités-Praticien Hospitalier (PU-PH) en Cardiologie à la Faculté de Médecine de Lille (Université de Lille, France) depuis 2023. Il a obtenu sa thèse de doctorat en sciences biologiques (PhD) en 2018 (Université Lille) et est habilité à diriger des recherches (HDR en 2021). Il a rejoint l’unité INSERM UMR1011, dirigée par le Pr Bart Staels depuis 2013. Dans cette équipe, Augustin Coisne est impliqué dans des projets de « recherche translationnelle cardiovasculaire » centrés sur la fonction, le métabolisme et le remodelage cardiaques chez des patients souffrant de diabète et/ou de cardiopathie valvulaire.
Le Pr. Augustin Coisne est également responsable de l’unité de cardiologie du service de Physiologie & Explorations Fonctionnelles CardioVasculaire (EFCV) du CHU de Lille depuis 2018. Il a effectué un stage post-doctoral au Clinical Trial Center et au Skirball Center for Innovation de la Cardiovascular Research Foundation à New York, NY, USA en 2021 (Dr Juan Granada).
Il est également coordonnateur du Comité Recherche et Innovation Valvulopathies du CHU de Lille. Il est coauteur d’une centaine d’articles, majoritairement dans le domaine de la recherche translationnelle et clinique concernant les maladies valvulaires et l’imagerie avec des publications en tant que premier auteur dans les revues European Heart Journal, JAMA Cardiology, JACC, JACC Cardiovascular Intervention, JACC Cardiovasc Imaging et Heart.
Il est membre du conseil d’administration de la Filiale d’Imagerie Cardiovasculaire de la de la Société Française de Cardiologue, ancien ambassadeur de France pour le programme Heart Imagers of Tomorrow (HIT) de l’Association européenne d’imagerie cardiovasculaire (EACVI), membre du Groupe Valves de la SFC et du PCR tricuspid focus group

PONTANA François
Fonction PU-PH – Radiologie et Imagerie Médicale
francois.pontana[@]chu-lille.fr
ORCID : 0000-0001-5316-7101


LEMESLE Gilles
PU-PH – Cardiologie
ORCID : 0000-0002-2917-9273
Institut Cœur Poumon - Dpt. de Cardiologie - Unité de soins intensifs cardiaques et laboratoire de cathétérisme - CHU de Lille - FRANCE.
Gilles Lemesle, est un cardiologue universitaire (thèse de médecine en 2007) sur un poste de professeur titulaire en cardiologie à la faculté de médecine de Lille depuis 2017. Il a effectué un fellowship à Washington DC en 2008-2009 (Pr Ron Waksman et Augusto Pichard, Washington Hospital Center, USA). Il a obtenu sa thèse de doctorat en sciences biologiques (PhD) en 2015 et est habilité à diriger des recherches (HDR en 2016). Il a rejoint l'unité INSERM UMR1011, dirigée par le Pr Bart Staels depuis 2016. Dans cette équipe, Gilles Lemesle mène des projets de " recherche translationnelle cardiovasculaire " centrés sur l'infarctus du myocarde, la maladie coronaire et la gestion des traitements antithrombotiques chez les patients coronariens avec ou sans diabète. Gilles Lemesle est également responsable du service des urgences cardiologiques et des soins intensifs de cardiologie au CHU de Lille depuis 2022.
Il est co-auteur de plus de 200 articles et a publié une quarantaine d’articles comme 1er auteur dans le domaine de la recherche translationnelle et clinique avec une thématique axée sur l'infarctus du myocarde, la maladie coronaire et la gestion des traitements antithrombotiques.
Il est dans ce cadre coordonnateur d’études randomisées et investigateur principal de nombreux essais.
Il est membre du groupe GRRC (Groupe de Réflexion en Recherche Cardiovasculaire, FRANCE) depuis 2013 et est maintenant président du groupe depuis 2024. Il est également membre du groupe FACT (French Alliance for Cardiovascular Trials, FRANCE) depuis 2016. Il est membre de la SFC (Société Française de Cardiologie), du GACI (Groupe Athérome coronaire et Cardiologie Interventionnelle), de l'ESC (European Society of Cardiology) et de l'EAPCI (European Association of Percutaneous Cardiovascular Intervention).

NINNI Sandro
MCU-PH – Cardiologie
ORCID : 0000-0001-6179-6098
Sandro Ninni est un cardiologue universitaire (thèse de médecine en 2016) sur un poste de professeur associé en cardiologie à la faculté de médecine de Lille (Université de Lille, France) depuis 2020. Il a obtenu sa thèse de doctorat en sciences biologiques (PhD) en 2021 et son habilitation à diriger les recherche (HDR en 2024). Il a rejoint l'unité INSERM UMR1011, dirigée par le Pr Bart Staels depuis 2017. Dans cette équipe, Sandro NINNI a développé des projets de " recherche translationnelle cardiovasculaire " axés sur l'arythmie cardiaque et son association avec la réponse inflammatoire et les troubles métaboliques.
Sandro NINNI est également impliqué dans le département de médecine cardiovasculaire avec une expertise spécifique dans le domaine des arythmies cardiaques et de l'électrophysiologie cardiaque. Sandro NINNI effectue également un stage post-doctoral à Montréal (Institut Cardiologique de Montréal, laboratoire du Dr Nattel) afin de développer de nouvelles compétences dans le domaine de l'électrophysiologie cellulaire.
Il a publié des articles dans le domaine de la (patho)physiologie cardiaque, et les arythmies cardiaques. Il est membre élu du comité scientifique de la Société Française de Cardiologie : Groupe de Réflexion sur la Recherche Cardiovasculaire depuis 2022.

TAZIBET Amine
Cardiologue - Etudiant en thèse de sciences
ORCID : 0009-0007-5564-6625
Amine Tazibet est jeune cardiologue (thèse de médecine en 2022) spécialisé dans la rythmologie et stimulation cardiaque. Il est inscrit en thèse de Sciences depuis 2023 avec un travail s’articulant autour de l’évaluation du remodelage atrial et le profil inflammatoire des patients, notamment l’hématopoïèse clonale. Il s’oriente vers une carrière hospitalo-universitaire avec un poste initial de Chef de Clinique Assistant au CHU de Lille à partir de novembre 2025.

WOITRAIN Eloïse
Ingénieur d’études
eloise.woitrain[@]pasteur-lille.fr
ORCID : 0000-0002-9913-9023
Eloïse Woitrain est ingénieur au CHU de Lille. Elle a obtenu son master Biologie-santé à l'université de Lille en 2013.
A la fin de ses études, elle a intégré l'unité INSERM UMR1011, dirigée par le Pr Bart Staels. Eloïse a d'abord rejoint l'équipe travaillant dans le domaine des pathologies métaboliques du foie pendant 5 ans. Elle s'est concentrée principalement sur l’exploration de nouveaux médicaments destinés à traiter la MASH en utilisant des modèles in vivo et in vitro pour tester l’efficacité et la sécurité de ces traitements. En 2018, Eloïse a rejoint l'équipe du Pr David Montaigne et participe à des projets de recherche translationnelle axés sur le métabolisme et le remodelage cardiaque chez des patients atteints de valvulopathie et/ou de diabète. En parallèle, elle participe à des projets de recherche centrés sur le remodelage cardiaque causé par des maladies métaboliques, en utilisant des modèles précliniques et cliniques.

WITOCKX Kimberly
Assistant ingénieur
kimberly.witockx[@]univ-lille.fr
ORCID : 0009-0003-9981-8127
Kimberly WITOCKX est assistant ingénieur. Elle est diplômée d’une Licence Professionnelle en innovations thérapeutiques et biotechnologies. Après une petite expérience au LFB de Lille (Laboratoire français du fractionnement et des biotechnologies), elle a poursuivi son parcours professionnel en intégrant Cerballiance, un laboratoire d’analyses médicales. En 2023, elle a intégré l’unité INSERM UMR1011, dirigée par le Pr Bart Staels et a rejoint le groupe du Pr David Montaigne. Elle participe aux expérimentations in vitro et in vivo tant sur le plan préclinique que clinique.
Nous avons démontré en 2018 que l'heure de la journée affecte les résultats cardiaques des patients avec des conséquences plus sévères lorsque le remplacement chirurgical de la valve aortique a été réalisé le matin par rapport à l'après-midi (Montaigne D, et al., Lancet. 2018).
Grâce à une collaboration avec les membres de l'équipe du consortium Leducq, nous avons étudié la spécificité des patients atteints d'hématopoïèse clonale (CHIP) qui bénéficient d'une chirurgie cardiaque. Nous avons montré que ces patients avaient un taux significativement plus élevé de fibrillation atriale postopératoire et un risque accru de complications cardiovasculaires majeures (décès cardiovasculaire, accident vasculaire cérébral, hospitalisation pour insuffisance cardiaque aiguë...) (Ninni S. et al., J Am Coll Cardiol. 2023).
En collaboration avec le Dr Jérémy Fauconnier de Montpellier, nous avons mis en évidence l'homéostasie calcique mitochondriale, et plus précisément le complexe uniporteur calcique mitochondrial (MCUC), comme un déterminant de la fibrillation auriculaire dans le syndrome métabolique et une cible thérapeutique attractive (Fossier L. et al., J Am Coll Cardiol 2022).
Notre équipe à développé une expertise sur les thématiques suivante :
- Imagerie cardiaque (échographie, IRM)
- Expérimentations in vivo (modèles de constriction de l’aorte, télémétrie, stimulation atriale transoesophagienne…)
- Expérimentations in vitro (culture cellulaire)
- Etude du phénotype cardiaque (histologie, expression génique et protéique, métabolisme énergétique du cardiomyocyte, marqueurs d’inflammation en technique de multiplexage)
- Analyse de la fonction mitochondriale (Oroboros, Sea Horse)
- Immunophénotypage (FACS / single cell RNAseq)
Liste des diffèrentes publications majeures du groupe coeur de l'équipe 1 :
Coisne A, Montaigne D, Aghezzaf S, Ninni S, Lemesle G, Sudre A, Lamblin N, Modine T, Vincentelli A, Juthier F, Leon MB, Granada JF, Bauters C. Clinical Outcomes According to Aortic Stenosis Management: Insights From Real-World Practice. J Am Heart Assoc. 2024 Nov 19;13(22):e036657. doi: 10.1161/JAHA.124.036657. Epub 2024 Nov 15. PMID: 39548024; PMCID: PMC11681392.
Aghezzaf S, Coisne A, Bauters C, Favata F, Delsart P, Coppin A, Seunes C, Schurtz G, Verdier B, Lamblin N, Tazibet A, Le Taillandier de Gabory J, Ninni S, Donal E, Lemesle G, Montaigne D. Feasibility and prognostic significance of ventricular-arterial coupling after myocardial infarction: the RIGID-MI cohort. Eur Heart J Cardiovasc Imaging. 2024 Apr 30;25(5):668-677. doi: 10.1093/ehjci/jead342. PMID: 38133627.
Ninni S, Dombrowicz D, de Winther M, Staels B, Montaigne D, Nattel S. Genetic Factors Altering Immune Responses in Atrial Fibrillation: JACC Review Topic of the Week. J Am Coll Cardiol. 2024 Mar 26;83(12):1163-1176. doi: 10.1016/j.jacc.2023.12.034. PMID: 38508850.
T. Rodrigues, V. Mishyn,Y. R. Leroux, L. Butruille, E. Woitrain, A. Barras, P.Aspermair, H. Happy, C. Kleber, R. Boukherroub, D. Montaigne, W. Knoll, S. Szunerits (2022). Highly performing graphene-based field effect transistor for the differentiation between mild-moderate-severe myocardial injury
. Nano Today, 2022 doi.org/10.1016/j.nantod.2022.101391
Montaigne D, Butruille L, Staels B. PPAR control of metabolism and cardiovascular functions. Nat Rev Cardiol. 2021 Dec;18(12):809-823. doi: 10.1038/s41569-021-00569-6. Epub 2021 Jun 14. PMID: 34127848. (Review)
Montaigne D, Marechal X, Modine T, Coisne A, Mouton S, Fayad G, Ninni S, Klein C, Ortmans S, Seunes C, Potelle C, Berthier A, Gheeraert C, Piveteau C, Deprez R, Eeckhoute J, Duez H, Lacroix D, Deprez B, Jegou B, Koussa M, Edme JL, Lefebvre P, Staels B. Daytime variation of perioperative myocardial injury in cardiac surgery and its prevention by Rev-Erbα antagonism: a single-centre propensity-matched cohort study and a randomised study. Lancet. 2018 Jan 6;391(10115):59-69. doi: 10.1016/S0140-6736(17)32132-3. Epub 2017 Oct 26. PMID: 29107324.
Montaigne D, Marechal X, Coisne A, Debry N, Modine T, Fayad G, Potelle C, El Arid JM, Mouton S, Sebti Y, Duez H, Preau S, Remy-Jouet I, Zerimech F, Koussa M, Richard V, Neviere R, Edme JL, Lefebvre P, Staels B. Myocardial contractile dysfunction is associated with impaired mitochondrial function and dynamics in type 2 diabetic but not in obese patients. Circulation. 2014 Aug 12;130(7):554-64. doi: 10.1161/CIRCULATIONAHA.113.008476. Epub 2014 Jun 13. PMID: 24928681.
Montaigne D, Marechal X, Lefebvre P, Modine T, Fayad G, Dehondt H, Hurt C, Coisne A, Koussa M, Remy-Jouet I, Zerimech F, Boulanger E, Lacroix D, Staels B, Neviere R. Mitochondrial dysfunction as an arrhythmogenic substrate: a translational proof-of-concept study in patients with metabolic syndrome in whom post-operative atrial fibrillation develops. J Am Coll Cardiol. 2013 Oct 15;62(16):1466-73. doi: 10.1016/j.jacc.2013.03.061. Epub 2013 May 1. PMID: 23644086.
Liste des diffèrents projets et financements du groupe coeur de l'équipe 1 :
1- Projet clinique TOMIS et POMI-AF financé par la bourse jeune chercheur de l'Agence Nationale pour la Recherche (ANR TOMIS-Leukocyte : ANR-CE14-0003-01) et le réseau LEAN 16CVD01 de la Fondation Leducq. Le projet est dédié à mieux comprendre les complications post-opératoires (par exemple, l'infarctus du myocarde, l'insuffisance cardiaque et la fibrillation auriculaire) après une chirurgie cardiaque, avec un intérêt particulier pour comprendre l'impact du moment de la journée de chirurgie sur les résultats.
2- Projet clinique Preci-Diab Heart : dans le cadre du National Center for Precision Diabetic Medicine www.precidiab.org et financé par l'Agence Nationale pour la Recherche française (ANR-18-IBHU-0001). Le projet est dédié à l'amélioration du phénotypage des patients grâce à de nouveaux biomarqueurs et à l'imagerie cardiaque afin d'adapter la médecine cardiaque personnalisée chez les patients diabétiques de type 2.
3- Projet RIGID-MI (PI Prof. G Lemesle) Ce projet clinique est dédié à une meilleure compréhension du remodelage cardiaque et des complications (ex. infarctus du myocarde, insuffisance cardiaque et fibrillation auriculaire) après un infarctus du myocarde.
4- Projet VALVENORD (PI Prof. C Bauters) Ce projet clinique vise à mieux comprendre le remodelage et les complications cardiaques (ex. infarctus du myocarde, insuffisance cardiaque et fibrillation auriculaire) chez les patients ambulatoires souffrant de sténose valvulaire aortique (de légère à sévère) dans les Hauts de France. Le projet est subventionné par la Fédération Française de Cardiologie.
5- Le projet translationnel CALMOS (coll. avec J Fauconnier Univ Montpellier) est financé par une subvention de l'Agence Nationale pour la Recherche (ANR CALMOS : ANR 18-CE17-0003-02). Ce projet est dédié à mieux comprendre le rôle des mitochondries cardiaques dans les arythmies cardiaques.
6- Le projet translationnel LivImmCar a pour objectif de mettre en évidence l'interaction de la stéatose hépatique associée à une dysfonction métabolique (MASH) et de ses altérations immunitaires avec le remodelage cardiaque chez les patients souffrant de maladies cardiovasculaires. Le projet est subventionné par la Fédération Française de Cardiologie et la Fondation pour la Recherche Médicale.
Liste des anciens membres du groupe Coeur :
Dr Laura Butruille -> Maitre de Conférence Universitaire à l'Université de Nantes