Thème 7 : ENDO-PLAST - Rôles de la plasticité dans les cellules endothéliales et reprogrammation métabolique dans les maladies, Equipe Emergente Atip-Avenir
Présentation de la thématique de recherche
L'endothélium joue un rôle indispensable dans tous les tissus, et son dysfonctionnement contribue à divers troubles cardiovasculaires, notamment l'athérosclérose, ainsi qu'au cancer. Cibler les vaisseaux sanguins dysfonctionnels représente une piste prometteuse pour le développement de thérapies visant à prévenir ou à traiter les maladies les plus répandues.
Nos recherches visent à caractériser le rôle du dysfonctionnement des cellules endothéliales (CE) dans l'apparition et la progression des maladies cardiovasculaires et du cancer. Plus précisément, nous nous concentrons sur la plasticité des CE et la reprogrammation métabolique associée en tant que facteurs de progression de la maladie.
En combinant des compétences multidisciplinaires et en utilisant des approches cellulaires et moléculaires avancées, ainsi que des modèles de souris transgéniques in vivo, notre équipe ENDO-PLAST s'efforce de déchiffrer les mécanismes complexes qui régulent la transdifférenciation pathologique des CE en cellules de type mésenchymateuses (transition endothéliale-mésenchymateuse, EndMT), dans le but d'identifier de nouveaux moyens de cibler ce processus. Nos travaux s'inscrivent dans une approche translationnelle visant, à long terme, à traduire nos découvertes en applications cliniques afin d'améliorer la prise en charge des patients atteints de maladies cardiovasculaires et de cancer.
Mots-clés
Biologie vasculaire ; cellules endothéliales ; plasticité endothéliale ; perméabilité vasculaire ; métabolisme ; récepteurs nucléaires ; hétérogénéité métabolique
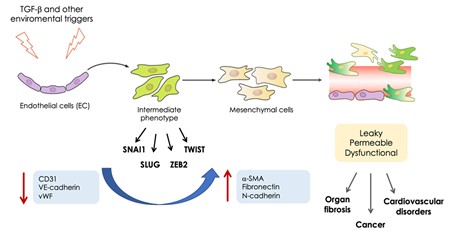
Processus EndMT : À la suite de stimuli environnementaux, notamment le TGF-b, l'hypoxie et le stress oxydatif, les CE perdent progressivement leur identité en régulant à la baisse les marqueurs endothéliaux (CD31, VE-cadhérine, facteur von Willebrand) et acquérent l'expression de marqueurs mésenchymateux (a-SMA, fibronectine, N-cadhérine) et de facteurs de transcription (SNAI1, SLUG, ZEB2, TWIST), ce qui entraîne un dysfonctionnement des vaisseaux.

Anna Rita Cantelmo, PhD, HDR
Cheffe d'équipe - CRCN - INSERM
anna-rita.cantelmo[@]univ-lille.fr
J’ai commencé mon voyage scientifique en réalisant ma thèse de doctorat dans le laboratoire du Dr. Adriana Albini au sein du « MultiMedica », (Milan, Italie), où j’ai travaillé sur le développement de stratégies innovantes pour cibler l’angiogenèse tumorale. Après ma thèse, j’ai rejoint le laboratoire du Pr. Peter Carmeliet au sein du « VIB-KUL », (Louvain, Belgique), où j’ai exploré le rôle du régulateur de la glycolyse PFKFB3 dans le métabolisme des cellules endothéliales et son impact sur l’angiogenèse et le cancer. Ces travaux ont abouti à des publications de qualités qui ont amélioré mon expertise dans la biologie vasculaire. En 2018, je suis arrivé en France, où j’ai obtenu un financement pour poursuivre mes recherches sur l’angiogenèse au sein de l’Université de Lille. Je suis bénéficiaire du prestigieux programme Atip-Avenir, et mon équipe est basée au sein de l'UMR1011 à l'Institut Pasteur de Lille, où nous intégrons la recherche fondamentale et translationnelle pour étudier comment les anomalies EC contribuent aux maladies cardiovasculaires.
Cyril Robil, MSc
Ingénieur d’étude sénior
cyril.robil[@]pasteur-lille.fr
Je suis ingénieur à l'Institut Pasteur de Lille depuis 2020. Je suis titulaire d'un master en biotechnologie de l'université de Lille et d'une licence en biologie/biochimie de l'université d'Orléans. Mes recherches précédentes portaient sur des projets liés à la COVID-19, notamment l'étude de la sénescence cellulaire et le rôle du microbiote intestinal dans le développement de la maladie. Au cours de cette période, j'ai géré plusieurs projets de recherche et participé à plusieurs collaborations scientifiques. Avant de rejoindre l'Institut Pasteur de Lille, j'ai travaillé comme technicienne chez GENFIT, où j'ai contribué au développement de thérapies pour les maladies du foie, en me spécialisant dans les analyses protéomiques et transcriptomiques. Au sein de l'équipe dirigée par le Dr Anna Rita Cantelmo, je soutiens les projets en cours par la planification expérimentale, la coordination technique et la gestion des ressources. Je participe à la conception et à l'exécution des expériences, à l'optimisation des protocoles, à l'analyse des données, à la supervision et à la formation des jeunes chercheurs, tout en coordonnant les opérations quotidiennes du laboratoire, notamment les ressources partagées, la commande de réactifs et le respect des normes de sécurité et de qualité.
Oksana Plu, MSc
Ingénieur d'étude
oksana.plu@pasteur-lille.fr
Après avoir obtenu une licence en chimie, j'ai obtenu un master en biologie-santé, avec une spécialisation en microbiologie et oncologie, à l'Université de Picardie Jules Verne. Au cours de mes stages, j'ai travaillé sur l'hétérogénéité tumorale dans le cancer de la vessie, ainsi que sur le rôle des espèces Lactobacillus dans l'inflammation et dans la colonisation par Candida albicans. Ces expériences m'ont permis de développer une solide expertise technique en microbiologie, en biologie moléculaire et cellulaire, et en techniques histologiques. En octobre 2025, j'ai rejoint l'équipe de recherche dirigée par le Dr Anna Rita Cantelmo en tant que technicienne de recherche. À ce titre, je participe à plusieurs projets de recherche, notamment ceux axés sur la protéine mitochondriale CHCHD4 et l'EndMT. Je contribue à la mise en œuvre et à l'optimisation des protocoles expérimentaux, j'apporte un soutien technique aux études in vitro et in vivo, et je participe à l'acquisition et à l'analyse des données.

Louay Bettaieb, PhD
Chercheur post-doctorant
Mes recherches portent sur la manière dont les cellules endothéliales reprogramment leur métabolisme au cours de la progression d'une maladie. J'ai obtenu mon master et mon doctorat à l'université de Lille au sein de l'équipe de recherche dirigée par le Dr Anna Rita Cantelmo, ce qui m'a permis d'obtenir mon doctorat en 2025. Mon projet porte sur le rôle du facteur d'importation des protéines mitochondriales CHCHD4 dans l'angiogenèse et sa contribution aux maladies cardiovasculaires. Mon travail combine des approches avancées de biologie moléculaire et cellulaire avec des modèles murins in vivo afin de disséquer comment la régulation mitochondriale dépendante du CHCHD4 contrôle la plasticité endothéliale et la fonction vasculaire. Grâce à des interactions avec des équipes de recherche translationnelle, je vise à établir un lien entre les mécanismes fondamentaux et les stratégies thérapeutiques ciblant le dysfonctionnement mitochondrial et les anomalies vasculaires, afin de contribuer à l'amélioration des résultats pour les patients.

Amani Machmouchi, MSc
Etudiante en thèse, Université de Lille
amani.machmouchi[@]univ-lille.fr
Passionné par la biologie et la recherche médicale, j'ai obtenu une licence en biologie à l'Université libanaise, suivie d'une licence en biologie animale et d'un master en recherche en immunologie. J'ai également suivi une formation complémentaire en administration de la santé. Je suis actuellement doctorante au sein de l'UMR1011 à l'Institut Pasteur de Lille, où je travaille sur le projet « Transition endothéliale-mésenchymateuse (EndMT) dans l'angiogenèse pathologique », avec un accent particulier sur l'athérosclérose et le cancer. Mes recherches visent à découvrir les mécanismes à l'origine de l'EndMT et à comprendre sa contribution au remodelage vasculaire et à la progression de la maladie. Mon travail intègre des modèles murins in vivo, notamment des approches basées sur des endotraceurs, ainsi que des techniques cellulaires et moléculaires pour étudier l'EndMT dans des contextes pathologiques. En parallèle, j'intègre des approches bioinformatiques, notamment la méta-analyse de jeux de données transcriptomiques accessibles au public, afin d'établir une signature génétique EndMT robuste et conservée dans différents modèles pathologiques. En combinant des études mécanistiques avec des modèles pertinents pour la maladie, mon objectif est d'identifier et d'exploiter de nouveaux facteurs EndMT afin de limiter le dysfonctionnement vasculaire dans l'athérosclérose et les maladies cardiovasculaires associées.

Evan Courmont, MSc
Etudiant en thèse, Université de Lille (Co-tutelle avec le Pr. Dimitra Gkika, CANTHER, Lille)
evan.courmont.etu[@]univ-lille.fr
Fascinée par les sciences, j'ai obtenu une licence en biologie cellulaire et physiologie en 2021, puis un master en biologie et santé (section oncologie) en 2023 à l'université de Lille. Depuis mon master, je travaille au sein de l'équipe de recherche dirigée par le Dr Anna Rita Cantelmo, où j'ai d'abord étudié le rôle des récepteurs nucléaires dans les cellules endothéliales et les fonctions vasculaires. Je poursuis actuellement mon doctorat en co-supervision avec Dimitra Gkika au laboratoire CANTHER (UMR9020 CNRS / UMR1277 Inserm). Mon travail combine des approches de biologie moléculaire et cellulaire avec des tests fonctionnels et des modèles pertinents pour la maladie afin de disséquer comment les voies de signalisation dépendantes du calcium contrôlent la plasticité endothéliale, les décisions relatives au destin cellulaire et le remodelage tissulaire. En intégrant la biologie vasculaire à la recherche sur les canaux ioniques, mon objectif est d'identifier de nouveaux mécanismes et de nouvelles cibles thérapeutiques pour limiter les maladies vasculaires et fibrotiques induites par l'EndMT.
Corina Birzoi, MSc
Etudiante en thèse, Université de Lille
corina.birzoi[@]pasteur-lille.fr
Après avoir obtenu une licence en biologie moléculaire et cellulaire et un master en biologie omique et systémique à l'université de Lille, j'ai effectué un stage axé sur la recherche sur les sarcomes, où j'ai acquis une expérience pratique des techniques avancées de spectrométrie de masse. Je poursuis actuellement un projet de doctorat intitulé « Le rôle de la protéine mitochondriale CHCHD4 dans la fonction endothéliale ». Ce projet étudie comment la régulation de l'homéostasie mitochondriale dans les cellules endothéliales, médiée par la CHCHD4, contribue au remodelage angiogénique dans le contexte de troubles métaboliques systémiques. Mon travail vise spécifiquement à déchiffrer comment la reprogrammation métabolique dépendante de la CHCHD4 module le comportement endothélial, l'intégrité vasculaire et les réponses angiogéniques adaptatives dans des conditions pathologiques. À l'aide d'une stratégie multidisciplinaire combinant des approches mécanistiques in vitro et des modèles murins in vivo de maladies métaboliques, j'étudie comment la perturbation spécifique à l'endothélium de la voie CHCHD4 influe sur les réseaux de signalisation angiogénique, la fonction mitochondriale et le remodelage vasculaire associés au dysfonctionnement métabolique.
Publications récentes:
Courmont E, Cantelmo AR. Calcium Signaling and Metabolic Reprogramming in Cancer: Mechanisms and Therapeutic Implications. Cold Spring Harb Perspect Biol. 2025.
La signalisation calcique lie étroitement la reprogrammation métabolique à la progression du cancer en remodelant la fonction mitochondriale, l'équilibre redox et les décisions relatives au destin cellulaire. Ce travail met en évidence la plasticité métabolique dépendante du calcium comme mécanisme central à l'origine de la croissance tumorale et de la résistance aux traitements, et examine son potentiel en tant que vulnérabilité thérapeutique.
Lebas M, Chinigò G, Courmont E, Bettaieb L, Machmouchi A, Goveia J, Beatovic A, Van Kerckhove J, Robil C, Angulo FS, Vedelago M, Errerd A, Treps L, Gao V, Delgado De la Herrán HC, Mayeuf-Louchart A, L'homme L, Chamlali M, Dejos C, Gouyer V, Garikipati VNS, Tomar D, Yin H, Fukui H, Vinckier S, Stolte A, Conradi LC, Infanti F, Lemonnier L, Zeisberg E, Luo Y, Lin L, Desseyn JL, Pickering JG, Kishore R, Madesh M, Dombrowicz D, Perocchi F, Staels B, Pla AF, Gkika D, Cantelmo AR. Integrated single-cell RNA-seq analysis reveals mitochondrial calcium signaling as a modulator of endothelial-to-mesenchymal transition. Sci Adv. 2024.
L'EndMT, essentielle au développement embryonnaire et liée aux maladies cardiovasculaires, reste difficile à moduler. À l'aide du séquençage d'ARN unicellulaire, nous avons identifié des signatures génétiques conservées de l'EndMT et découvert que l'absorption mitochondriale du calcium est un facteur clé de l'EndMT. L'inhibition du transporteur unipolaire du calcium mitochondrial (MCU) a empêché l'EndMT in vitro, et la suppression du MCU a bloqué l'activation mésenchymateuse dans un modèle de maladie. Des niveaux élevés de MCU ont également été observés chez des patients atteints d'ischémie critique des membres. Ces résultats suggèrent que le MCU pourrait constituer une cible thérapeutique potentielle pour le traitement des maladies liées à l'EndMT
Nouvelles de l'équipe:
Félicitations à Louay pour avoir soutenu avec succès sa thèse de doctorat. Il s'agit d'une étape importante pour lui, mais aussi pour notre équipe, car Louay est notre tout premier doctorant diplômé ! Bravo, Louay ! Nous te souhaitons bonne chance pour la suite de ton parcours scientifique, qui se poursuivra encore quelque temps avec nous (décembre 2025).
Amani partira bientôt pour un court séjour de recherche en Allemagne, où elle rejoindra le laboratoire du professeur Lena Conradi à l'université de Göttingen afin d'acquérir une expertise dans le domaine des organoïdes humains. Un grand merci au programme Precision Health de l'École Doctorale Biologie Santé Université de Lille pour son soutien financier (novembre 2025).
Bravo à nos étudiants pour leur participation à la première édition de la Journée des doctorants de l'IPL, et en particulier à Evan pour avoir présenté nos travaux sur l'EndMT dans la fibrose (novembre 2025).
Nos étudiants Amani et Evan participeront à la Fête de la Science, où ils s'engageront activement auprès du public pour présenter nos activités de recherche et promouvoir la curiosité scientifique et le dialogue. Amusez-vous bien ! (octobre 2025).
Notre post-doctorant Mauro, ainsi que d'autres membres de l'unité, ont participé à la Journée européenne du patrimoine. Ils ont expliqué le rôle d'un chercheur et les principaux axes de recherche de l'UMR1011 à un public non initié (octobre 2024).
Notre doctorant Louay Bettaieb passera bientôt trois mois à Louvain, en Belgique, dans le cadre de son programme de mobilité doctorale. Il rejoindra le laboratoire du professeur Peter Carmeliet à la VIB-KUL afin d'acquérir des connaissances supplémentaires en matière de vascularisation et de métabolisme et de générer les données finales nécessaires à la finalisation de son travail de doctorat (septembre 2024).
Notre équipe possède une solide expertise en biologie vasculaire, avec un accent particulier sur la caractérisation des (dys)fonctions des CE dans des conditions physiologiques et pathologiques. Nous avons mis en place des protocoles permettant d'isoler des CE primaires à partir de cordons ombilicaux humains prélevés sur des donneurs au CHU de Lille, ce qui nous permet de générer des cultures de CE primaires pour des études fonctionnelles in vitro. En parallèle, nous avons développé plusieurs lignées de souris transgéniques qui nous permettent d'étudier la dynamique et la plasticité des CE in vivo, à la fois dans des conditions homéostatiques et dans des modèles pathologiques. Notre expertise comprend l'utilisation d'approches de traçage de lignées, de systèmes Cre-lox inductibles et de modèles pathologiques cardiovasculaires et cancéreux pertinents. Au niveau moléculaire, l'équipe est spécialisée dans les approches omiques avancées, notamment le séquençage d'ARN en vrac et de cellules uniques, l'analyse intégrative des données et la validation fonctionnelle des voies candidates. Nous élargissons actuellement notre expertise en transcriptomique spatiale et avons reçu une formation spécifique sur le pipeline de pointe Visium HD de 10x Genomics, qui permet une cartographie spatiale haute résolution de l'hétérogénéité endothéliale au sein de tissus complexes.
Publications :
Lebas M, Chinigò G, Courmont E, Bettaieb L, Machmouchi A, Goveia J, Beatovic A, Van Kerckhove J, Robil C, Angulo FS, Vedelago M, Errerd A, Treps L, Gao V, Delgado De la Herrán HC, Mayeuf-Louchart A, L’homme L, Chamlali M, Dejos C, Gouyer V, Garikipati VNS, Tomar D, Yin H, Fukui H, Vinckier S, Stolte A, Conradi LC, Infanti F, Lemonnier L, Zeisberg E, Luo Y, Lin L, Desseyn JL, Pickering J, Kishore R, Madesh M, Dombrowicz D, Perocchi F, Staels B, Pla AF, Gkika D, Cantelmo AR.
Integrated single-cell RNA-seq analysis reveals mitochondrial calcium signaling as a modulator of endothelial-to-mesenchymal transition
Sci Adv. 2024 Aug 9;10(32)
Dejos C, Gkika D, Cantelmo AR.
The Two-Way Relationship Between Calcium and Metabolism in Cancer.
Front. Cell Dev. Biol., 2020 Nov 13;8:573747.
Veys K, Fan Z, Ghobrial M, Bouché A, García-Caballero M, Vriens K, Conchinha NV, Seuwen A, Schlegel F, Gorski T, Crabbé M, Gilardoni P, Ardicoglu R, Schaffenrath J, Casteels C, De Smet G, Smolders I, Van Laere K, Abel ED, Fendt SM, Schroeter A, Kalucka J, Cantelmo AR, Wälchli T, Keller A, Carmeliet P, De Bock K.
Role of the GLUT1 Glucose Transporter in Postnatal CNS Angiogenesis and Blood-Brain Barrier Integrity.
Circ Res. 2020 Jul 31;127(4):466-482.
Eelen G*, Dubois C*, Cantelmo AR, Goveia J, Brüning U, DeRan M, Jarugumilli G, van Rijssel J, Saladino G, Comitani F, Zecchin A, Rocha S, Chen R, Huang H, Vandekeere S, Kalucka J, Lange C, Morales-Rodriguez F, Cruys B, Treps L, Ramer L, Vinckier S, Brepoels K, Wyns S, Souffreau J, Schoonjans L, Lamers WH, Wu Y, Haustraete J, Hofkens J, Liekens S, Cubbon R, Ghesquière B, Dewerchin M, Gervasio FL, Li X, van Buul JD, Wu X, Carmeliet P. *equal contribution
Role of glutamine synthetase in angiogenesis beyond glutamine synthesis.
Nature. 2018 Sep;561(7721):63-69.
Conradi LC*, Brajic A*, Cantelmo AR*, Bouché A, Kalucka J, Pircher A, Brüning U, Teuwen LA, Vinckier S, Ghesquière B, Dewerchin M, Carmeliet P. *equal contribution
Tumor vessel disintegration by maximum tolerable PFKFB3 blockade.
Angiogenesis. 2017 Nov;20(4):599-613.
Cantelmo AR*, Conradi LC*, Brajic A*, Goveia J*, Kalucka J, Pircher A, Chaturvedi P, Hol J, Thienpont B, Teuwen LA, Schoors S, Boeckx B, Vriens J, Kuchnio A, Veys K, Cruys B, Finotto L, Treps L, Stav-Noraas TE, Bifari F, Stapor P, Decimo I, Kampen Kim, De Bock K, Haraldsen G, Schoonjans L, Rabelink T, Eelen G, Ghesquière, B, Rehman J, Lambrechts D, Malik AB, Dewerchin M, & Carmeliet P. *equal contribution
Inhibition of the glycolytic activator PFKFB3 in endothelial cells induces tumor vessel normalization, impairs metastasis and improves chemotherapy
Cancer Cell. 2016 Dec 12;30(6):968-985.
Nous recherchons un bioinformaticien spécialisé dans l'analyse multi-omique, notamment la métabolomique et l'omique spatiale. Pour en savoir plus, consultez notre profil LinkedIn (septembre 2025).
Nous sommes toujours intéressés par l'accueil d'étudiants en licence et en master et acceptons les candidatures de doctorants motivés et fortement intéressés par la biologie vasculaire, la plasticité des cellules endothéliales et les mécanismes pathologiques associés.
Anna Rita CANTELMO
Institut Pasteur de Lille, U1011-EGID
1 rue du Professeur Calmette
59000 LILLE - France
e-mail: anna-rita.cantelmo[@]univ-lille.fr
office: +33 3 20 87 71 48
Alumni
Mauro Vedelago, PhD (2024-2025)
Fabiola Silva, PhD (2024-2025)
Mohamed Chamlali, PhD (2021-2023)
Wiliam Masselin (2022-2024)
Camille Dejos, PhD (2019-2021)
Mathilde Lebas, MSc (2018-2022)
Stagiaires
Mohamed Nasreldin, University of Lille, MSc training (2026)
Cyril Benda, University of Rennes, BSc training (2025)
Chamseddine Amarouche, University of Lille, BSc training (2025)
Segolene Tandrayen, University of Angers, BSc training (2025)
Alina Errerd, Erasmus +, German Cancer Research Center (DKFZ), MSc training (2024)
Camille Lafeuille, Apprentis Chercheur, high school student (2023)
Victorea Banza, University of Lille, BSc training (2023)
Evan Courmont, University of Lille, MSc training (2023)
Louay Bettieb, University of Lille, MSc training (2022)
Afaf Ennahal, University of Lille, BSc training (2021)